Kamu
pasti pernah melihat besi. Nah, besi itu sebenarnya termasuk jenis unsur logam.
Lalu apa sebenarnya unsur itu? Pada kesempatan kali ini kita akan membahas
pengertian unsur.
Pengertian Unsur
Unsur
adalah suatu zat tunggal yang tidak dapat diuraikan lagi menjadi zat lain yang
lebih sederhana dengan reaksi kimia biasa. Unsur merupakan zat murni.
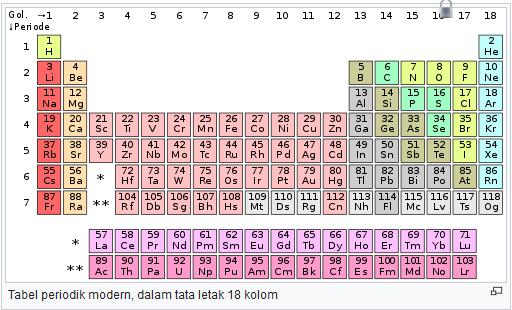
Jumlah
unsur-unsur yang dikenal sampai saat ini mencapai 118 unsur. Dari jumlah tersebut,
92 unsur di antaranya merupakan unsur yang ditemukan di alam, sedangkan sisanya
merupakan unsur buatan yang dibuat oleh para ahli di labolatorium. Berdasarkan
sifat-sifatnya unsur dibedakan menjadi unsur logam, unusr metaloid (semilogam)
dan unsur nonlogam (bukan logam).
1. Unsur Logam
Unsur
logam mempunyai sifat-sifat sebagai berikut.
a. Mengilap
b. Dapat direntang menjadi kawat atau ditempa menjadi
lempengan
c. Bersifat konduktor (penghantar listrik dan panas yang
baik)
d. Pada suhu kamar berwujud padat, kecuali logam raksa,
sesium, fransium, dan galium yang berwujud cair.
Beberapa
contoh unsur logam diantaranya litium, natrium, kalium, rubidium, magnesium,
kalsium, barium, besi, tembaga, emas, dan perak.
2. Unsur Metaloid
Unsur
metaloid mempunyai sifat-sifat sebagai berikut
a. Lebih rapuh dari logam, tetapi kurang rapuh dibandingkan
nonlogam
b. Bersifat semikonduktor (penghantar panas yang lebih baik
daripada nonlogam, tetapi kurang baik daripada logam).
c. Beberapa metaloid berkilauan seperti logam
Beberapa
unsur metaloid, di antaranya boron, silikon, germanium, arsen, dan antimon.
3. Unsur Nonlogam
Unsur
nonlogam mempunyai sifat-sifat sebagai berikut
a. Pada suhu kamar umumnya berwujud gas, namun ada juga yang
berwujud padat atau cair.
b. Bersifat isolator (tidak dapat menghantarkan panas dan
listrik), kecuali beberapa unsur nonlogam seperti karbon yang bersifat
konduktor.
c. Umumnya tidak mengilap
d. Tidak dapat ditempa
Beberapa
contoh unsur nonlogam, di antaranya belerang, oksigen, nitrogen, fosforus, dan
karbon.
Lambang Unsur
Untuk
membedakan unsur yang satu dan lainnya, setiap unsur diberi nama yang berbeda
dengan nama unsur lainnya. Akan tetapi, untuk lebih mempermudah penulisan
masing-masing unsur, dibuat suatu lambang tertentu untuk setiap unsur. Lambang
ini disebut lambang unsur. Lambang
unsur yang satu berbeda dengan lambang unsur lainnya.
Lambang
unsur yang sampai sekarang kita gunakan, ditemukan atau diciptakan oleh Jons
Jakob Berzelius, seorang ahli kimia yang berasal dari Swedia. Menurut
Berzelius, suatu unsur diberi nama dengan mengambil huruf pertama nama Latin
unsur tersebut yang ditulis dengan huruf besar.
Sebagai
contoh, unsur nitrogen memiliki nama Latin nitrogenium,
maka lambang unsurnya adalah N. Unsur hidrogen memiliki nama Latin hidrogenium, maka lambang unsurnya
adalah H. Karena jumlah unsur yang ditemukan lebih banyak dari jumlah huruf
abjad yang hanya 26 huruf dan terdapat unsur-unsur yang dimulai dengan huruf
pertama yang sama, maka beberapa unsur dilambangkan menggunakan huruf pertama
(huruf besar) dan salah satu huruf (huruf kecil) yang ada pada nama unsur
tersebut.
Contoh
Penulisan Lambang Unsur
1. Perak memiliki nama Latin argentum, maka lambang unsurnya adalah Ag
2. Emas memiliki nama Latin aurum, maka lambang unsurnya adalah Au
3. Besi memiliki nama Latin ferrum, maka lambang unsurnya adalah Fe
4. Klorin memiliki nama Latin chlorium, maka lambang unsurnya adalah Cl
Beberapa Unsur Penting dan Lambang
Unsurnya
Berikut
ini adalah beberapa contoh unsur-unsur dan lambang unsurnya.
Unsur
Logam
|
No.
|
Nama Latin
|
Nama Indonesia
|
Lambang Unsur
|
|
1.
|
Aluminium
|
Aluminium
|
Al
|
|
2.
|
Argentum
|
Peral
|
Ag
|
|
3.
|
Aurum
|
Emas
|
Fe
|
|
4.
|
Barium
|
Barium
|
Ba
|
|
5.
|
Bismuth
|
Bismut
|
Bi
|
|
6.
|
Calcium
|
Kalsium
|
Ca
|
|
7,
|
Chromium
|
Kromium
|
Cr
|
|
8.
|
Cuprum
|
Tembaga
|
Cu
|
|
9.
|
Ferrum
|
Besi
|
Fe
|
|
10.
|
Hydrargyrum/
Mercurium
|
Air Raksa
|
Hg
|
|
11.
|
Magnesium
|
Magnesium
|
Mg
|
|
12.
|
Manganum
|
Mangan
|
Mn
|
|
13.
|
Natrium
|
Natrium
|
Na
|
|
14.
|
Nicculum
|
Nikel
|
Ni
|
|
15.
|
Platinium
|
Platina
|
Pt
|
|
16.
|
Plumbum
|
Timbal
|
Pb
|
|
17.
|
Stannum
|
Timah
|
Sn
|
|
18.
|
Stibium
|
Antimon
|
Sb
|
|
19.
|
Zincum
|
Zink
|
Zn
|
Unsur
Nonlogam
|
No.
|
Nama Latin
|
Nama Indonesia
|
Lambang Unsur
|
|
1.
|
Argon
|
Argon
|
Ar
|
|
2.
|
Arsenikum
|
Arsen
|
As
|
|
3.
|
Bromium
|
Bromin
|
Br
|
|
4.
|
Carbonium
|
Karbon
|
C
|
|
5.
|
Clorium
|
Klorin
|
Cl
|
|
6.
|
Fluorium
|
Fluorin
|
F
|
|
7,
|
Hydogenium
|
Hidrogen
|
H
|
|
8.
|
Helium
|
Helium
|
He
|
|
9.
|
Iodium
|
Iodin
|
I
|
|
10.
|
Nitrogenium
|
Nitrogen
|
Ni
|
|
11.
|
Oxygenium
|
Oksigen
|
O
|
|
12.
|
Phosphorus
|
Fosforus
|
P
|
|
13.
|
Radon
|
Radon
|
Rn
|
Pengertian Senyawa
Senyawa
adalah zat tunggal yang secara kimia dapat diuraikan lagi menjadi zat-zat yang
lebih sederhana. Senyawa terbentuk dari gabungan dua atau lebih unsur yang
berbeda. Senyawa dapat diuraikan secara kimia menjadi unsur-unsurnya.
Ciri-ciri
senyawa adalah sebagai berikut.
1. Merupakan zat tunggal
2. Terbentuk dari dua unsur atau lebih yang berbeda jenis
dengan perbandingan tertentu dan tetap.
3. Sifat senyawa berbeda dengan sifat-sifat unsur
penyusunnya
4. Senyawa dapat diuraiakan menjadi unsur-unsurnya melalui
proses kimia
Salah
satu contoh senyawa adalah air. Air terbentuk dari unsur hidrogen dan unsur
oksigen. Misalnya, air berwujud cair, sedangkan unsur hidrogen dan oksigen
berwujud gas. Secara kimia, air dapat diuraikan menjadi gas hidrogen dan gas
oksigen kembali, misalnya dengan suatu proses yang disebut elektrolisis.
Contoh
senyawa lainnya adalah sebagai berikut.
1. Gula, terbentuk dari unsur karbon, unsur nitrogen, dan
unsur oksigen
2. Asam klorida, terbentuk dari unsur hidrogen dan unsur
klorin
3. Karbon dioksida, terbentuk dari unsur karbon dan unsur
oksigen
Pengertian Campuran
Campuran
adalah penggabungan dua zat murni atau lebih yang masih mempunyai sifat sifat
asalnya dan tidak mempunyai komposisi tertentu. Campuran terdiri atas tiga
bentuk, yaitu larutan, koloid, dan suspensi. Pada pembahasan kali ini, kita
akan mempelajari tentang larutan serta mengetahui sifat asam, basa, dan gaea,
yang dimiliki setiap larutan.
Larutan
adalah campuran homogen (serba sama) yang terdiri atas dua atau lebih zat.
Sebagai contoh, larutan gula. Pada larutan tersebut, kita dapat memperoleh
kembali butiran-butiran kristal gula dalam air dengan cara menguapkan
pelarutnya, yaitu air, melalui cara pemanasan. Saat semua air dalam larutan
telah menguap, gula akan mengkristal kembali membentuk butiran-butiran gula.
Prosesnya disebut pengkristalan atau kristalisasi.
Pemisahan Campuran
Campuran
dapat dipisahkan sehingga diperoleh kembali dua atau lebih zat yang membentuk
campuran. Ada beberapa cara untuk memisahkan campuran, di antaranya dengan
penyaringan (filtrasi), penyulingan (distilasi), kromatografi, dan
kristalisasi,
1. Penyaringan (Filtrasi)
Penyaringan
(filtrasi) didasarkan pada perbedaan jenis zat atau besar kecilnya zat yang ada
dalam campuran. Di dalam labolatorium, pemisahan ini biasanya menggunakan
corong dan kertas saring.
Cara
filtrasi biasanya digunakan pada contoh berikut ini.
a. Pemisahan kotoran yang ada pada larutan gula.
b. Menyaring air sungai untuk keperluan air bersih
Zat
hasil penyaringan disebut filtrat,
sedangkan zat sisa dari penyaringan disebut residu.
2. Penyulingan (distilasi)
Penyulingan
(distilasi) adalah pemisahan campuran zat yang didasarkan pada perbedaan titik
didih zat-zat cair yang ada dalam campuran.
Penyulingan
dapat dilakukan, misalnya untuk memunirkan air laut sehingga diperoleh air
tawar. Air laut yang akan dimurnikan dimasukkan ke dalam suatu wadah, yang disebut
labu distilasi atau labu alas bulat. Labu berisi air kemudian didihkan, yang
menguap hanya air. Garam tidak ikut menguap karena titik didihnya jauh lebih
tinggi dari air. Uap air kemudian melewati tabung pendingin dan mengembun
menjadi air tawar ke dalam labu penampung.
Zat hasil distilasi disebut distilat, sedangkan zat zat sisa yang
tertinggal dalam distilat disebut residu.
Penyulingan ini biasanya dilakukan dalam suatu alat yang disebut distilator.
3. Kromatografi
Kromatografi
adalah pemisahan yang didasarkan pada perbedaan distribusi zat-zat yang akan
dipisahkan terhadap fase diam berupa zat penyerap (adsorben). Distribusi
zat-zat yang akan dipisahkan tersebut oleh fase gerak. Adsorpsi adalah peristiwa penyerapan pada permukaan adsorben.
Kromatografi
dapat digunakan untuk memisahkan zat-zat warna yang terdapat pada tinta.
Kromatografi ini dapat dilakukan dengan menggunakan kertas saring sebagai
penyerap atau fase diam. Tinta yang diinginkan zat-zat warnanya ditotolkan pada
salah satu ujung kertas saring dengan jarak sekitar 1 cm dari ujung kertas.
Kertas saring kemudian dimasukkan ke dalam suatu wadah berisi air yang berperan
sebagai fase gerak. Tinggi air dalam wadah sekitar 0,5 cm. Air akan merembes
naik melalui kertas saring melewati tinta.
Zat-zat warna yang diserap lebih
kuat oleh kertas akan tertahan di bagian bawah kertas, sedangkan zat-zat warna
yang kurang kuat diserap oleh kertas akan larut dengan air dan ikut merembes
naik ke atas bersama air.
4. Kristalisasi
Kristalisasi
adalah pemisahan campuran yang dilakukan untuk memisahkan campuran padat dan
cair dengan cara menguapkan zat cairnya. Cara kristalisasi digunakan pada
contoh berikut.
a. Membuat garam dari air laut
b. Membuat gula tebu dari cairan tebu
5. Sublimasi
Submilasi
adalah pemisahan campuran yang didasarkan pada komponen campuran dengan salah
satu komponen dapat menyublim (perubahan zat padat menjadi gas), sedangkan
komponen yang lain tidak dapat menyublim.
Contoh
sublimasi adalah padatan iodin atau kapur barus
Bagaimana
sobat, sudah pahamkan penjelasan tentang Pengertian Unsur, Senyawa, dan Campuran
serta Pemisahannya. Kalau sudah paham,jangan lupa ikuti postingan
kami selanjutnya dan share artikel kami. Terima kasih.



No comments
silahkan berkomentar secara bijak dan sesuai dengan topik pembahasan